助力科研,碧云天蛋白定量与裂解液产品荣登Cell杂志
碧云天产品助力肺腺癌蛋白质组分子图谱解析2020年7月9日在《Cell》杂志在线发表了中国科学院上海药物研究所 谭敏佳研究员团队联合军事科学院军事医学研究院、国家蛋白质科学中心(北京) 贺福初院士团队、 汪宜研究员团队,国家癌症中心/中国医学科学院肿瘤医院 程书钧院士、 肖汀研究员团队,上海交通大学 李婧教授等团队的最新合作研究成果“Integrative Proteomic Characterization of Human Lung Adenocarcinoma”,该研究对103例临床肺腺癌(LUAD)患者的肿瘤组织及癌旁组织进行了全面分析,包括蛋白质组学、磷酸化蛋白质组学、转录组学和全基因组测序分析。构建了基于蛋白质组的肺腺癌分子图谱全景,并根据不同的临床表现和分子特征将LUAD患者分为了三种亚型。该研究首次在蛋白质水平系统绘制肺腺癌的分子图谱,并发现了中国人群肺腺癌两个主要基因TP53和EGFR突变的分子特征,提出了LUAD药物治疗的潜在靶点,证实了HSP 90β作为LUAD预后指标的可能性,为LUAD的精准诊断和治疗提供了更为全面的理论支持。

研究人员对103个肺腺癌患者临床样本及对应的癌旁组织进行了多组学水平的全方位分析,鉴定出了11119个蛋白产物和22564个磷酸化修饰位点。通过对比肿瘤组织与癌旁组织的数据,研究人员发现二者之间存在明显的边界,说明在肺腺癌的发生和发展过程中存在着蛋白质组学的异常变化。通过整合分析蛋白质多组学数据,研究人员发现仅有1.2%的非同义SNVs和小片段indel引发了蛋白质水平表达的变化,这些数据说明在肺腺癌疾病发展过程中其转录组学、蛋白质组学和磷酸化组学具有各自的特征,将其适当整合,有助于更好地理解并发现新的具有重要功能的基因变化。
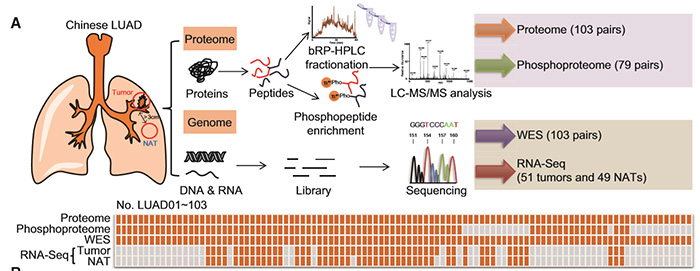
Fig. 1A Overview of the experimental design and the number of samples for proteomics, phosphoproteomics, WES, and RNA-seq analyses

Fig. 2B-C Integrative Omics Analyses of LUAD Samples
研究人员通过对比中国LUAD图谱数据和TCGA发布的白种人LUAD图谱得知,不同种族的肺腺癌癌基因存在遗传学差异。中国人群肺腺癌主要存在两个基因突变的分子特征,分别是EGFR和TP53,同时这种突变还与患者的预后情况密切相关。若患者同时具有EGFR和TP53两种突变,其通常具有不良预后,而且会出现氧化磷酸化、脂肪酸代谢在内的多种代谢相关信号通路表达下调和致瘤信号通路表达的上调。

Fig. 3C-D Proteomics Characteristics of TNM Stage I LUAD and LUADs with EGFR/TP53 Mutation
同时,研究人员根据所得数据将肺腺癌分为三个蛋白质组亚型(I 型、II 型、III 型)。其中,I 型(Environment and metabolism, EM-H)与细胞代谢和肿瘤微环境密切相关,临床信息显示该型主要为临床早期人群,并且预后最为良好;III 型(Proliferation and proteasome, PP)与细胞稳态及增殖密切相关,其主要为临床中后期人群,呈现出肿瘤分化程度较低,基因突变负荷较高等特征,并且预后最差;II 型则是 I 型和 III 型的过渡状态,这部分人群预后程度介于 I 型和 III 型之间,并且II 型患者的EGFR突变频率更高,而III 型的肿瘤突变负荷最高。蛋白质组分析数据表明,HSP 90β可能是预测LUAD预后状况的理想标志物。
在研究中,研究人员选用了碧云天的BCA protein assay kit用于WB实验中组织样品蛋白含量的测定。


| 产品编号 | 产品名称 | 产品包装 |
| P0009 | BCA蛋白浓度测定试剂盒(增强型) | 5000次 |
| P0010 | BCA蛋白浓度测定试剂盒(增强型) | 500次 |
| P0010S | BCA蛋白浓度测定试剂盒(增强型) | 200次 |
| P0011 | BCA蛋白浓度测定试剂盒 | 5000次 |
| P0012 | BCA蛋白浓度测定试剂盒 | 500次 |
| P0012S | BCA蛋白浓度测定试剂盒 | 200次 |
论文链接:
Jun-Yu Xu,. et al. Integrative Proteomic Characterization of Human Lung Adenocarcinoma. Cell 2020
https://doi.org/10.1016/j.cell.2020.05.043
碧云天产品助力肿瘤免疫治疗研究
2020年6月23日,《Cell》杂志在线发表了南方医科大学、中山大学附属第八医院的徐洋教授、付雪梅教授团队、加州大学旧金山分校王磊教授团队、中国科学院理化技术研究所杭州研究院的王谦研究员最新合作研究成果“Developing Covalent Protein Drugs via Proximity-Enabled Reactive Therapeutics”,该研究构建了一种接近启用反应性疗法(proximity-enabled reactive therapeutics, PERx),用其来产生共价蛋白药物。研究人员利用该技术得到了经非天然氨基酸氟-硫-L-络氨酸(fluorosulfate-L-tyrosine,FSY)修饰的PD-1蛋白(PD-1(FSY)),该PD-1(FSY)能够与PD-L1共价交联,不可逆地阻断肿瘤细胞表面PD-L1与T细胞表面PD-1结合。并且在免疫抑制微环境中,PD-1(FSY)蛋白药物比传统抗体药物更有效地清除实体肿瘤。该研究成果为共价蛋白药物的研发奠定了基础,并展现了其在肿瘤免疫治疗领域的应用前景。

研究人员认为在蛋白药物的结合位点整合进一段具有潜在生物活性的Uaas能够增强该蛋白分子药物与作用靶点结合的特异性,为了验证这一理论,研究团队选取了PD-1/PD-L1免疫检查点进行测试。根据人PD-1/PD-L1复合物的蛋白结构,分别在PD-1的Gln75、Asp77和Ala129位点共价连接了FSY,经过一系列表达纯化,最终得到了三种PD-1突变体——PD-1(FSY),并且经过质谱分析证实FSY已被整合进PD-1分子的特定位点。
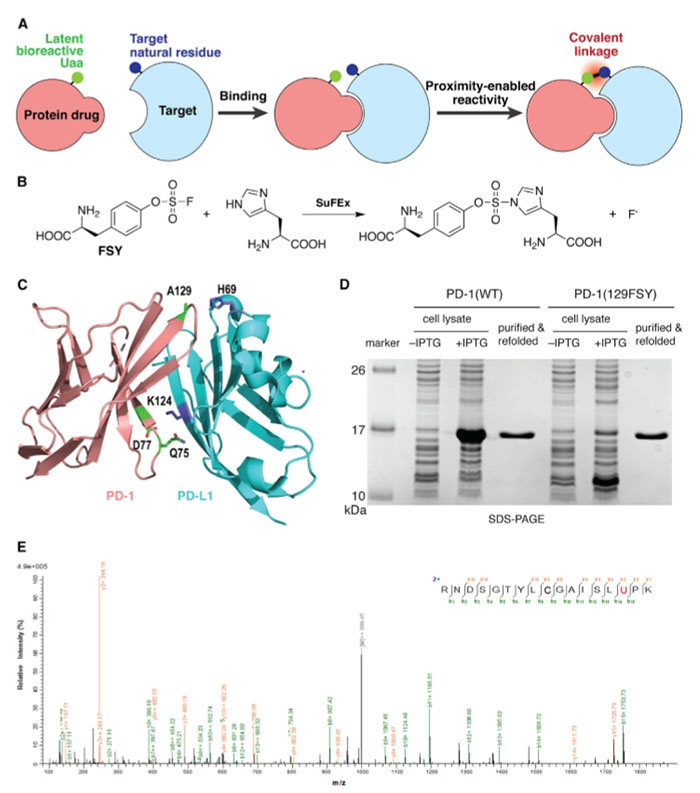
Figure 1. Developing Covalent Protein Drugs via PERx
为了证实PD-1(FSY)能否与PD-L1进行共价结合,研究人员又进行了一系列体内外实验。研究人员首先将PD-1(FSY)与PD-L1共同孵育,同时以PD-1(WT)和PD-L1作为对照,结果显示,PD-1(75FSY)和PD-1(129FSY)均与PD-L1形成了稳定的共价复合物,且PD-1(129FSY)(43%±4%)比PD-1(129FSY)(16%±2%)具有更高的结合效率。随后研究人员又选取H460和U87细胞进行进一步验证,结果显示PD-1(FSY)与细胞表面PD-L1具有良好的结合效率,并且随着PD-1(FSY)剂量的增加,结合效率也随之增加。研究人员将两种细胞接种在免疫缺陷小鼠体内并注入PD-1(WT)和PD-1(FSY),可以观察到,PD-1(FSY)与PD-L1形成了共价结合,而PD-1(WT)则并没有与PD-L1结合,上述结果均证实改造后的PD-1变体PD-1(FSY)具有良好的PD-L1结合能力。
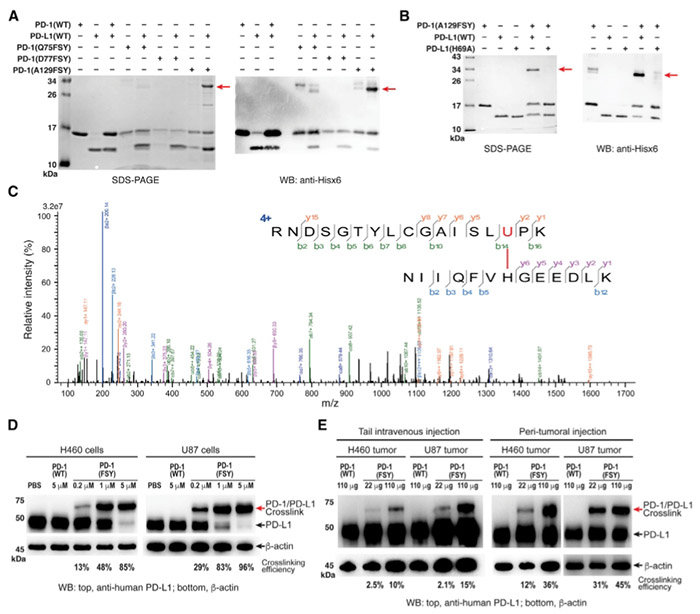
Figure 2. PD-1(FSY) Covalently Bound to Its Ligand PD-L1 via Proximity-Enabled Reactivity of the Latent Bioreactive Uaa FSY
研究人员证实了PD-1(FSY)与atezolizumab类似,在体外都能够增强T细胞活化,随后构建了人源化免疫缺陷小鼠肿瘤模型,进一步验证PD-1(FSY)体内作用效果。分别给予两组小鼠一定剂量的 PD-1(FSY)和 PD-1(WT),结果显示 PD-1(FSY)能够明显抑制肿瘤生长, PD-1(FSY)组的瘤块重量明显轻于PD-1(WT)组,减少PD-1(FSY)的使用剂量后依旧能取得良好的抗肿瘤效果。PD-1(FSY)与atezolizumab具有类似的作用作用,而使用剂量却仅为atezolizumab的一半。同时,PD-1(FSY)还能够增强CAR-T细胞在肿瘤组织的浸润能力,提高其活性,增强体内抗肿瘤效果。

Figure 4. PD-1(FSY) Inhibited Tumor Growth More Effectively Than PD-1(WT) in PBMCTumor Xenograft Mouse Model
该研究成功证明了PD1(FSY)蛋白药物具有理想的清除实体肿瘤的作用,显示了共价蛋白质药物在肿瘤免疫治疗中的临床应用前景;也进一步显示了人源化免疫系统实体肿瘤模型在肿瘤免疫治疗药物有效性及安全性评价中的优势。
在验证PD-1(FSY)能否与细胞表面PD-L1结合时,研究者们选用了碧云天的RIPA裂解液和BCA protein assay kit用于细胞裂解和后续蛋白定量。

相关产品:
| 产品编号 | 产品名称 | 产品包装 |
| P0009 | BCA蛋白浓度测定试剂盒(增强型) | 5000次 |
| P0010 | BCA蛋白浓度测定试剂盒(增强型) | 500次 |
| P0010S | BCA蛋白浓度测定试剂盒(增强型) | 200次 |
| P0011 | BCA蛋白浓度测定试剂盒 | 5000次 |
| P0012 | BCA蛋白浓度测定试剂盒 | 500次 |
| P0012S | BCA蛋白浓度测定试剂盒 | 200次 |
| P0013C | RIPA裂解液(中) | 100ml |
| P0013D | RIPA裂解液(弱) | 100ml |
| P0013B | RIPA裂解液(强) | 100ml |
| P0013K | RIPA裂解液(强, 无抑制剂) | 100ml |
| P0013E | RIPA裂解液(强中弱套装) | 共150ml |
论文链接:
Qingke Li, et al. Developing Covalent Protein Drugs via Proximity-Enabled Reactive Therapeutics. Cell, 2020.
https://doi.org/10.1016/j.cell.2020.05.028