


 微信在线咨询
微信在线咨询

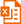
| 产品编号 | 产品名称 | 产品包装 | 产品价格 |
| D7255FT | Easy-Load™ PCR Master Mix (Green, 2X) (试用装) | 20次 | .00元 |
| D7255-1ml | Easy-Load™ PCR Master Mix (Green, 2X) | 100次 | 36.00元 |
| D7255-4ml | Easy-Load™ PCR Master Mix (Green, 2X) | 400次 | 112.00元 |
| D7255-20ml | Easy-Load™ PCR Master Mix (Green, 2X) | 2000次 | 440.00元 |
| D7255-100ml | Easy-Load™ PCR Master Mix (Green, 2X) | 10000次 | 1759.00元 |
碧云天的Easy-Load™ PCR Master Mix(Green, 2X)是一种使用特别便捷的含有蓝色和橙色染料(电泳位置分别约4kb和50bp)的2倍浓度的PCR预混液,含有2X Taq DNA Polymerase、2X PCR Buffer、2X dNTP和2X Loading Buffer,只需加入模板DNA、引物和水即可进行PCR扩增,并且扩增完毕后可以直接上样电泳。主要适用于cDNA或基因组DNA等的常规PCR扩增,特别适合于定性或半定量的PCR扩增,也可用于长度小于2kb的DNA片段的扩增和克隆。
Easy-Load™ PCR Master Mix(Green, 2X)中已经含有所有的通用组分,用户只需自备引物、模板DNA和水即可进行PCR扩增。大大简化了PCR操作,使操作更加快捷,也减少了PCR操作过程中可能导致的污染,使PCR的重复性更好。
Easy-Load™ PCR Master Mix(Green, 2X)可以扩增出长达8kb的片段,但通常更适合用于扩增2kb以下的DNA片段。
本产品中加入了蓝色和橙色的电泳示踪染料(整体呈现绿色),其在浓度为1%琼脂糖胶中的迁移位置分别大约位于4kb和50bp处。PCR结束后可直接进行电泳检测,无需再添加上样缓冲液。蓝色和橙色示踪染料不会影响对相应DNA条带的观察和检测。
本产品稳定性高,经测试,反复冻融15次后对PCR的扩增效果无显著影响。反复冻融15次前后,使用不同引物扩增100-1500bp间不同长度目的片段的效果如图1所示。
每毫升Easy-Load™ PCR Master Mix若用于50微升的PCR反应体系,足够用于40个反应;若用于20微升的PCR反应体系,足够用于100个反应。
包装清单:
| 产品编号 | 产品名称 | 包装 |
| D7255FT | Easy-Load™ PCR Master Mix (Green, 2X) (试用装) | 0.2ml |
| D7255-1ml | Easy-Load™ PCR Master Mix (Green, 2X) | 1ml |
| D7255-4ml | Easy-Load™ PCR Master Mix (Green, 2X) | 1ml×4 |
| D7255-20ml | Easy-Load™ PCR Master Mix (Green, 2X) | 1ml×20 |
| D7255-100ml | Easy-Load™ PCR Master Mix (Green, 2X) | 1ml×100 |
| — | 说明书 | 1份 |
保存条件:
-20℃保存至少一年有效。适当避免反复冻融。如需频繁使用,可取适量存放于4℃,至少3天内有效。
注意事项:
由于PCR反应非常灵敏,可使目的基因扩增超过1000万倍,在设置PCR反应时请注意避免微量待扩增DNA的污染,并尽量考虑设置不加模板的空白对照以确认是否有待扩增DNA的污染。
Taq DNA polymerase在PCR过程中每个循环的出错几率约为2.2×10-5,对于大于1kb的DNA片段的克隆推荐使用出错几率更低的DNA聚合酶,例如Pfu DNA polymerase、BeyoTaq DNA polymerase等。对于普通的PCR或RT-PCR进行定性或定量检测,Taq DNA polymerase是最佳选择。
尽管本产品经过15次反复冻融后仍具有和冻融前几乎相同的PCR扩增效果,但仍宜适当避免反复冻融本产品,多次反复冻融可能使产品性能下降。
使用本产品前,一定要完全融化,并上下颠倒轻轻混匀后才能使用,并尽量避免产生气泡。
本产品仅限于专业人员的科学研究用,不得用于临床诊断或治疗,不得用于食品或药品,不得存放于普通住宅内。
为了您的安全和健康,请穿实验服并戴一次性手套操作。
使用说明:
1. PCR反应体系的设置:
a. 室温融解Easy-Load™ PCR Master Mix (Green, 2X),上下颠倒轻轻混匀后低速离心数秒。
b. 参考下表在冰浴上设置PCR反应体系:
| 试剂 | 最终浓度 | 体积 | 体积 |
| 双蒸水或Milli-Q水 | - | (21-x)μl | (8.4-y)μl |
| 模板DNA | 10pg-1μg | xμl | yμl |
| 引物混合物(10μM) | 0.8μM | 4μl | 1.6μl |
| Easy-Load™ PCR Master Mix (Green, 2X) | 1X | 25μl | 10μl |
| 总体积 | - | 50μl | 20μl |
注意:(a) 通常引物的终浓度为0.2μM时可获得良好的检测效果,也可以根据情况在0.1-1.0μM范围内调整引物的终浓度。扩增效率不高的情况下,可提高引物的浓度;发生非特异性反应时,可降低引物浓度。
color:#666666; (b) 对于不同类型的模板在50μl反应体积中推荐用量如下:
哺乳动物基因组DNA:0.1-1μg;大肠杆菌基因组DNA:10-100ng;质粒DNA:0.1-10ng。过多的模板DNA容易导致非特异性的PCR产物。
c. 用移液器轻轻吹打混匀或轻微Vortex混匀,室温离心数秒,使液体积聚于管底。
d. 如果所使用的PCR仪有热盖则省略本步骤。如果PCR仪没有热盖,则在管内滴入一滴矿物油(mineral oil,ST275)。
e. 把设置好的PCR反应管置于PCR仪上,开始PCR反应。
2. PCR反应参数的设置可以参考如下示例:
STEP1(起始变性): 94℃ 3min
STEP2(变性): 94℃ 30sec
STEP3(退火): 55℃ 30sec
STEP4(延伸): 72℃ 1min
STEP5(循环): Go To STEP2 for 30cycles
STEP6(最终延伸): 72℃ 10min
STEP7(临时保存): 4℃ forever
注意:
a. PCR反应的设置需根据模板、引物、PCR产物的长度和GC含量等条件的不同,设定不同的PCR反应条件包括温度、时间和循环数等。
b. STEP4(延伸)的时间设置需根据PCR产物的长度进行设置,通常每kb产物的延伸时间为1分钟。例如PCR产物的长度为1kb,则延伸时间可以设置为1分钟,PCR产物的长度为2kb,则延伸时间可以设置为2分钟,以此类推。
c. 对于初次进行的PCR,为尽量确保可以扩增出预期的PCR产物,可以把循环数设置为35。对于需进行半定量或定量的PCR反应循环数一定要进行适当优化,使PCR反应没有达到平台期。
3. 结果检测:PCR结束后直接取5-10μl进行电泳检测,无需添加上样缓冲液。
常见问题:
1. PCR产物非常少或没有特异性条带。
a. 引物设计不佳是PCR过程中最常见的问题。请选择适当的引物设计软件进行引物设计,注意引物的GC含量、二级结构、二聚体、退火温度、长度、特异性等方面的问题。在加入酶切位点等的引物中,一定要注意加入酶切位点等后整条引物的GC含量、二级结构、二聚体、退火温度、长度、特异性等方面的问题。在原有引物效果不佳的情况并且阳性对照引物可以正常工作的情况下,可以考虑更换引物。
b. 待扩增片段GC含量偏高。GC含量较高的情况下PCR会变得相对比较困难,此时可以使用适合扩增高GC含量DNA片段的GC-rich buffer,并相应地根据GC-rich buffer的要求或说明调整PCR反应参数的设置。
c. 长片段扩增。尽管Taq DNA polymerase可以扩增最长达8kb的DNA片段,但大多数时候比较适合扩增2-3kb以下的片段,更长片段的扩增推荐使用其它更适合长片段扩增的DNA聚合酶。
d. PCR反应设置时在室温进行容易导致非特异性条件。推荐在冰浴上设置PCR反应。
e. 由于引物存在一定的二级结构或存在一定的引物二聚体,或引物偏短,导致退火效果不佳。此时可以采用Touch down等方法进行退火,通常采用从65℃逐步缓慢降温到55℃或50℃的方法,使退火更加充分。
f. 退火温度不佳,需要优化。如果有温度梯度PCR仪,则可以设置退火的温度梯度,摸索退火的最佳温度。如果没有温度梯度PCR仪,则可以通过多次PCR反应摸索最佳的退火温度。
g. 延伸时间不足。可按照每1kb片段延伸1分钟进行设置,对于较难扩增的片段可以设置为每1kb片段延伸1.5-2分钟。
h. 待扩增片段GC含量较高或长度较长,变性不够充分。可以调节起始变性条件至95℃ 1min甚至95℃ 2-4min。
i. 在不同PCR仪上进行PCR反应,避免有时PCR仪出现问题。
j. 循环数不足,适当延长PCR的循环数。通常循环数最高不必超过40,常用的循环数范围为25-35。
k. 模板含量太低,适当加大模板量,或采用巢式PCR(nested PCR)或二次PCR。巢式PCR即为在原先设计的PCR引物内侧再设计一对PCR引物,然后对第一次PCR产物进行稀释后再进行一次PCR扩增,这样一方面可以起到扩增作用,同时也可以从第一次PCR产物中扩增出特异性条带。二次PCR则为比较简单地用原有引物对第一次PCR产物进行稀释后再进行一次PCR扩增,可以起到扩增作用,但不能去除非特异性条带。
l. 模板中含有抑制PCR反应的物质,可以用适当的DNA纯化方法例如柱纯化等纯化模板DNA。
m. 当产生较多非特异性条带时,可以适当提高退火温度。
n. 注意设置适当的阳性对照和阴性对照通常会有很大帮助。
相关产品:









 微信在线咨询
微信在线咨询












