|
|||||||||
产品简介
产品简介:
| 产品编号 | 产品名称 | 产品包装 | 产品价格 |
| P0309 | 神经氨酸酶抑制剂筛选试剂盒 | 100次 | 920.00元 |
神经氨酸酶抑制剂筛选试剂盒(Neuraminidase Inhibitors Screen Kit)是一种用荧光法快速高灵敏度高通量筛选神经氨酸酶抑制剂的试剂盒。
禽流感病毒在其外壳上有两种糖蛋白,一种是haemagglutinin,简称HA,另一种是neuraminidase,简称NA,也称唾液酸酶(sialidase)。目前治疗H5N1型禽流感的常见药物包括瑞士罗氏制药公司生产的Oseltamivir (Tamifu,达菲为其商品名)和葛兰素史克公司(GlaxoSmithKline)生产的Zanamivir (Relenza,瑞乐砂为其商品名),这两种药物都是neuraminidase的抑制剂。但达菲价格昂贵,普通百姓很难承受。并且达菲生产能力有限,如果发生较大规模的禽流感疫情,该药物的供给量有限。另外,在一些禽流感疫情中已经发现了达菲耐受的禽流感病毒,在达菲的临床测试中就发现存在一些对达菲耐受的禽流感病毒。Zanamivir不能口服,使应用范围受到限制。因此,寻找新的神经氨酸酶抑制剂作为治疗禽流感的药物非常迫切。希望本试剂盒能有助于寻找到更好的价廉物美的禽流感药物。
试剂盒中提供了纯化的神经氨酸酶和可以被神经氨酸酶催化产生荧光的底物,并且对神经氨酸酶的用量和底物的使用量进行了优化。不仅能检测出IC50很低的抑制剂,也能检测出IC50较高的抑制剂。
本试剂盒可以筛选溶解于水的抑制剂,也可以筛选溶解于甲醇、乙醇、DMSO的抑制剂。其它溶剂未经测试。
用于96孔板检测时,一个包装的本试剂盒可以检测100个样品或标准品。
包装清单:
产品编号 |
产品名称 |
包装 |
P0309-1 |
神经氨酸酶检测缓冲液 |
10ml |
P0309-2 |
神经氨酸酶 |
1ml |
P0309-3 |
神经氨酸酶荧光底物 |
1ml |
P0309-4 |
Milli-Q水 |
1.2ml |
― |
说明书 |
1份 |
保存条件:
-20℃保存,一年有效。神经氨酸酶荧光底物需避光保存。
注意事项:
神经氨酸酶和神经氨酸酶荧光底物尽量避免反复冻融。
试剂盒中所用溶液溶解后4℃保存,两天有效。如果两天内不能全部用完,建议尽早把留作以后使用的神经氨酸酶和神经氨酸酶荧光底物适当分装后-70℃保存,-20℃冻存也可,但有效期会较短。其余试剂直接-20℃或-70℃保存即可。
需使用荧光酶标仪,并需自备专门用于荧光酶标仪荧光检测的96孔荧光酶标板。或使用可以检测小体积样品的荧光分光光度计。使用荧光分光光度计时参考荧光酶标板的操作方法。
由于荧光检测非常灵敏,测定出来的荧光强度有时容易产生波动。一方面要避免灰尘等掉入检测孔中产生荧光干扰,另一方面所有检测最好在同一块检测板上做双份平行检测甚至三份平行检测。
本产品仅限于专业人员的科学研究用,不得用于临床诊断或治疗,不得用于食品或药品,不得存放于普通住宅内。
为了您的安全和健康,请穿实验服并戴一次性手套操作。
使用说明
使用说明:
1. 标准曲线检测的准备(参考表1):
a. 在96孔荧光酶标板内每孔加入70微升神经氨酸酶检测缓冲液。
b. 每孔再分别加入0、1、2、5、7.5、10微升神经氨酸酶。
c. 每孔再加入0-20微升Milli-Q水使每孔总体积为90微升。
2. 样品检测的准备(参考表1):
a. 在96孔荧光酶标板内每孔加入70微升神经氨酸酶检测缓冲液。
b. 每孔再加入10微升神经氨酸酶。
c. 每孔再加入0-10微升待筛选的神经氨酸酶抑制剂样品。
d. 每孔再加入0-10微升Milli-Q水使每孔总体积为90微升。
3. 检测(参考表1):
a. 振动混匀约1分钟。
b. 37oC孵育2分钟使抑制剂和神经氨酸酶充分相互作用,标准曲线孔也一起孵育。
c. 每孔加入10微升神经氨酸酶荧光底物。
d. 再振动混匀约1分钟。
e. 37℃孵育30分钟后进行荧光测定。激发波长为322nm,发射波长为450nm。
如果受仪器所限,不能设置前述波长,激发波长在310-335nm,发射波长在430-470nm也有良好
的检测效果。不同仪器的荧光检测灵敏度有所不同,孵育时间可根据实际的荧光读数进行适当调
整。当荧光读数偏低时,可以延长孵育时间(例如延长时间至1、2或4小时),以提高检测灵敏
度。
表1.检测体系的设置
|
标准曲线 |
样品 |
神经氨酸酶检测缓冲液 |
70 μl |
70 μl |
神经氨酸酶 |
0-10 μl |
10 μl |
待测样品 |
- |
0-10 μl |
Milli-Q水 |
0-20 μl |
0-10 μl |
神经氨酸酶荧光底物 |
10 μl |
10 μl |
总体积 |
100 μl |
100 μl |
4. 计算:
a. 根据标准曲线可以计算出样品对于神经氨酸酶的抑制百分比。对于检测发现有效的抑制剂,通过
检测该
抑制剂的剂量效应就可以测定出该抑制剂的IC50。
b.本试剂盒检测Oseltamivir acid的抑制效果如图1所示,IC50约为200μM。因为Oseltamivir phos
phate即达菲,需要在体内代谢成Oseltamivir acid才有良好的效果,所以Oseltamivir phosph
ate和Zanamivir用本试剂盒检测时,IC50都会显著高于200μM。
注意:神经氨酸酶活性检测体系中的IC50和病毒检测体系中的IC50存在较大差别。Oseltamivir
acid对于禽流感病毒的IC50根据文献报道在nM级别。因此如果能在神经氨酸酶活性检测体系中
筛选到IC50比较接近200μM的抑制剂时,就可能有非常重要的意义了。
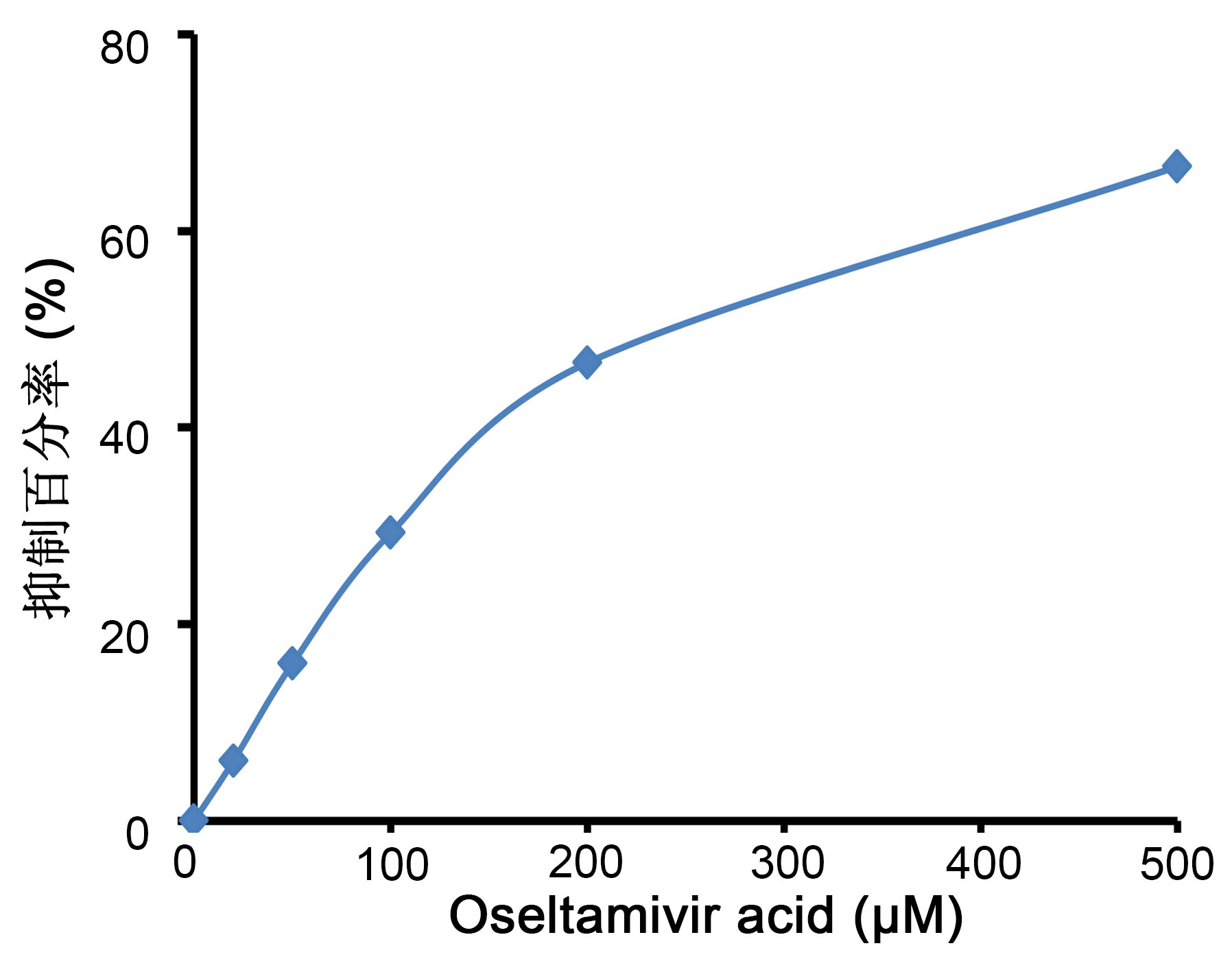
图1. 本试剂盒检测Oseltamivir acid的抑制效果。本图仅作参考,不同的样品不同的检测条
件,实际测定获得结果可能和上图有较明显的差别。
产品图片
相关产品
相关论文
使用本产品的相关论文:
1. Liu Y, Jing F, Xu Y, Xie Y, Shi F, Fang H, Li M, Xu W.
Design, synthesis and biological activity of thiazolidine-4-carboxylic acid derivatives
as novel influenza neuraminidase inhibitors.
Bioorg Med Chem. 2011 Apr 1;19(7):2342-8.
2. Liu S, Li R, Zhang R, Chan CC, Xi B, Zhu Z, Yang J, Poon VK, Zhou J, Chen M, Münch J,
Kirchhoff F, Pleschka S, Haarmann T, Dietrich U, Pan C, Du L, Jiang S.
CL-385319 inhibits H5N1 avian influenza A virus infection by blocking viral entry.
Eur J Pharmacol. 2011 Jun 25;660(2-3):460-7.
3. Liu Y, Zhang L, Gong J, Fang H, Liu A, Du G, Xu W.
Design, synthesis, and biological activity of thiazole derivatives as novel influenza
neuraminidase inhibitors.
J Enzyme Inhib Med Chem. 2011 Aug;26(4):506-13.
4. Yang J, Zhang F, Li J, Chen G, Wu S, Ouyang W, Pan W, Yu R, Yang J, Tien P.
Synthesis and antiviral activities of novel gossypol derivatives.
Bioorg Med Chem Lett. 2012 Feb 1;22(3):1415-20.
5. Liu S, Yan J, Xing J, Song F, Liu Z, Liu S.
Characterization of compounds and potential neuraminidase inhibitors from the n-butanol
extractof Compound Indigowoad Root Granule using ultrafiltration and liquid
chromatography-tandem mass spectrometry.
J Pharm Biomed Anal. 2012 Feb 5;59:96-101.
6. Yang J, Chen G, Li LL, Pan W, Zhang F, Yang J, Wu S, Tien P.
Synthesis and anti-H5N1 activity of chiral gossypol derivatives and its analogs
implicated by a viral entry blocking mechanism.
Bioorg Med Chem Lett. 2013 May 1;23(9):2619-23.
7. He J, Qi WB, Wang L, Tian J, Jiao PR, Liu GQ, Ye WC, Liao M.
Amaryllidaceae alkaloids inhibit nuclear-to-cytoplasmic export of ribonucleoprotein
(RNP) complex of highly pathogenic avian influenza virus H5N1.
Influenza Other Respir Viruses. 2013 Nov;7(6):922-31.
8. Wu J, Chen G, Xu X, Huo X, Wu S, Wu Z, Gao H.
Seven new cassane furanoditerpenes from the seeds of Caesalpinia minax.
Fitoterapia. 2014 Jan;92:168-76.
9. Yang J, Yang JX, Zhang F, Chen G, Pan W, Yu R, Wu S, Tien P.
Design, synthesis and biological evaluation of small molecular polyphenols as entry
inhibitors against H(5)N(1).
Bioorg Med Chem Lett. 2014 Jun 15;24(12):2680-4.
10.Song G, Shen X, Li S, Li Y, Liu Y, Zheng Y, Lin R, Fan J, Ye H, Liu S.
Structure-activity relationships of 3-O-β-chacotriosyl ursolic acid derivatives as novel
H5N1 entry inhibitors.
Eur J Med Chem. 2015 Mar 26;93:431-42.
11.Song G, Shen X, Li S, Si H, Li Y, Luan H, Fan J, Liang Q, Liu S.
Discovery of 3-O-β-chacotriosyl oleanane-type triterpenes as H5N1 entry inhibitors.
RSC Adv. 2015 5; 39145-39154.
苏ICP备06009238号 |